Aleaciones con memoria de forma en aplicaciones biomédicas
1 Introducción
1.1 Antecedentes
Las aleaciones con memoria de forma (SMA) son materiales compuestos por dos o más elementos metálicos que presentan efectos de memoria de forma (SME) mediante termoelasticidad y transformaciones de fase martensítica y sus inversiones. Las aleaciones con memoria de forma son los materiales con mejores prestaciones de memoria de forma entre los materiales con memoria de forma. Hasta la fecha, se han descubierto más de 50 tipos de aleaciones con efectos de memoria de forma.
Las aleaciones con memoria de forma presentan efectos de memoria de forma. Por ejemplo, cuando un muelle fabricado con una aleación con memoria de forma se coloca en agua caliente, su longitud se alarga inmediatamente. Cuando se introduce en agua fría, recupera inmediatamente su forma original. Los muelles de aleación con memoria de forma pueden utilizarse para controlar la temperatura del agua en las tuberías de los cuartos de baño: cuando la temperatura del agua es demasiado alta, la función de "memoria" regula o corta el suministro de agua para evitar quemaduras. También pueden utilizarse para crear dispositivos de alarma contra incendios y mecanismos de seguridad para equipos eléctricos. En caso de incendio, el muelle de aleación con memoria de forma se deforma, activando el sistema de alarma contra incendios para lograr el propósito de alertar. Además, los muelles de aleaciones con memoria de forma pueden colocarse dentro de válvulas de calefacción para mantener la temperatura ambiente, abriendo o cerrando automáticamente las válvulas cuando la temperatura baja o sube demasiado. El efecto de memoria de forma de las aleaciones con memoria de forma también se aplica ampliamente en diversos activadores de sensores de temperatura.

Fig. 1 Aplicaciones médicas del nitinol
Otra propiedad importante de las aleaciones con memoria de forma es la pseudoelasticidad (también conocida como superelasticidad), que se manifiesta como una capacidad de recuperación de la deformación significativamente mayor que la de los metales ordinarios bajo una fuerza externa. Es decir, la gran deformación generada durante la carga se recupera tras la descarga. Esta propiedad ha encontrado una amplia aplicación en medicina, reducción de vibraciones en edificios y en la vida cotidiana. Por ejemplo, los huesos artificiales antes mencionados, los dispositivos de presión para fijación ósea y los aparatos de ortodoncia dental. Las monturas de gafas fabricadas con aleaciones con memoria de forma pueden soportar deformaciones mucho mayores que los materiales ordinarios sin romperse (esto no se debe al efecto de memoria de forma, en el que a la deformación le sigue un calentamiento para recuperar la forma).
Las aleaciones con memoria de forma (SMA) tienen amplias aplicaciones en el campo de la medicina clínica, como huesos artificiales, dispositivos de presión para fijación ósea, aparatos de ortodoncia dental, diversos stents endovasculares, dispositivos de embolización, dispositivos de reparación cardiaca, filtros de trombos, guías de intervención y suturas quirúrgicas. Las aleaciones con memoria de forma desempeñan un papel insustituible en la medicina moderna. Las aleaciones con memoria de forma también están estrechamente relacionadas con nuestra vida cotidiana.
El desarrollo de las aleaciones con memoria de forma tuvo su origen en el descubrimiento en 1932 por Arne Ölander del efecto "memoria" en aleaciones de oro y cadmio. En 1963, el equipo de Buehler del Laboratorio Naval de Artillería de EE.UU. confirmó este fenómeno en aleaciones de níquel-titanio: los materiales deformados plásticamente por debajo de su temperatura de transición recuperan espontáneamente su forma original cuando se calientan por encima de un umbral crítico (por ejemplo, >40°C), impulsados por una transformación martensítica inversa activada térmicamente. En 1969 se produjeron avances industriales con los acoplamientos de tuberías de NiTi a prueba de fugas en la hidráulica aeronáutica y una antena lunar de NiTi predeformada que se autoexpandió al calentarse con energía solar durante la misión Apolo 11, superando las limitaciones de la carga útil. Investigaciones posteriores desarrollaron sistemas de NiTi multicomponente (por ejemplo, TiNiCu, TiNiFe) junto con SMA basados en cobre y hierro, permitiendo aplicaciones transformadoras en biomedicina, energía y automatización.
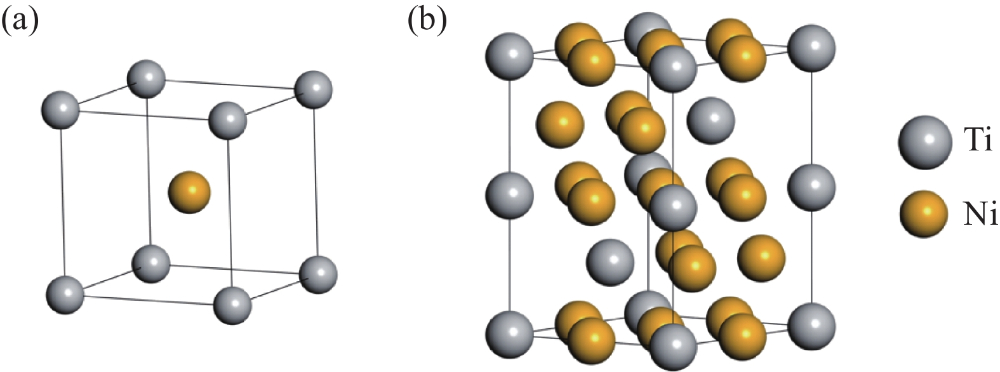
Fig. 2 Estructura cristalina del nitinol
La aleación con memoria de forma basada en Ti-Ni es la más útil de todas las aleaciones con memoria de forma. Las propiedades únicas de las aleaciones de níquel-titanio se derivan de la transformación de fase reversible entre la fase austenítica (alta temperatura/estado sin carga, estructura cúbica estable) y la fase martensítica (baja temperatura/estado con carga, estructura hexagonal fácilmente deformable). Entre sus características principales se incluyen: efecto de memoria de forma (la deformación martensítica seguida de un calentamiento hasta la temperatura crítica restaura la forma de la fase madre), superelasticidad no lineal (la transformación de fase martensítica inducida por la tensión permite una deformación recuperable del 8%, rompiendo las limitaciones de la ley de Hooke), sensibilidad a la temperatura oral (la fuerza ortodóncica aumenta con el aumento de la temperatura, acelerando el movimiento dental pero dificultando un control preciso), excelente biocompatibilidad (el óxido de titanio de la superficie inhibe la liberación de iones de níquel), y suave amortiguación de las vibraciones de la fuerza ortodóncica (la plataforma de la curva de descarga es plana, con una amplitud de vibración de sólo el 50% de la del alambre de acero inoxidable). Basados en la regulación por transformación de fases, los arcos de alambre de ortodoncia han evolucionado a lo largo de cinco generaciones: desde los alambres metálicos tradicionales (década de 1940) → aleaciones estabilizadas por martensita (década de 1960, baja rigidez, sin memoria) → aleaciones activadas austeníticas (década de 1980, superelasticidad de fuerza constante) → aleaciones activadas martensíticas (década de 1990, memoria de forma y superelasticidad activadas por temperatura corporal, logrando una "activación de forma-intraoral a temperatura ambiente") → aleaciones optimizadas termodinámicamente (década de 2000, activadas por encima de 40 °C, proporcionando una fuerza continua extremadamente débil para pacientes con enfermedad periodontal).
1.2 El atractivo de la AME en el ámbito médico
El atractivo de las aleaciones con memoria de forma (SMA) en el campo médico reside en la sinergia única entre sus propiedades materiales y los requisitos clínicos.
Las SMA de grado médico, representadas por el Nitinol (NiTi), presentan una composición casi equiatómica (50 at.% de níquel, 50 at.% de titanio). Los ajustes precisos de la composición permiten controlar los efectos de superelasticidad y memoria de forma. El nitinol superelástico experimenta una transformación martensítica inducida por la tensión, lo que permite obtener deformaciones recuperables de hasta el 8,0% (Fig. 1). Su curva de tensión-deformación presenta una meseta definida, superando al acero inoxidable 316 de uso médico convencional.
Las principales ventajas clínicas abarcan tres dimensiones:
1. Innovación funcional: La superelasticidad permite la miniaturización y la autoexpansión en dispositivos mínimamente invasivos (por ejemplo, stents vasculares, filtros);
2. 2. Biocompatibilidad: El Nitinol de superficie optimizada cumple las normas de seguridad biológica para implantes.
3. 3. Avance quirúrgico: Los dispositivos accionados por SMA (por ejemplo, arcos de alambre para ortodoncia, oclusores cardiovasculares/neurovasculares) mejoran la precisión del procedimiento al tiempo que reducen el traumatismo tisular.
Especialmente en radiología intervencionista, la superelasticidad del nitinol permite afrontar los retos críticos de la flexibilidad de los dispositivos, la resistencia al acodamiento y la adaptación dinámica in vivo, impulsando avances transformadores en terapias mínimamente invasivas. Este artículo examina con más detalle el potencial de aplicación médica de la SMA y las estrategias de gestión de riesgos para los implantes de Nitinol.
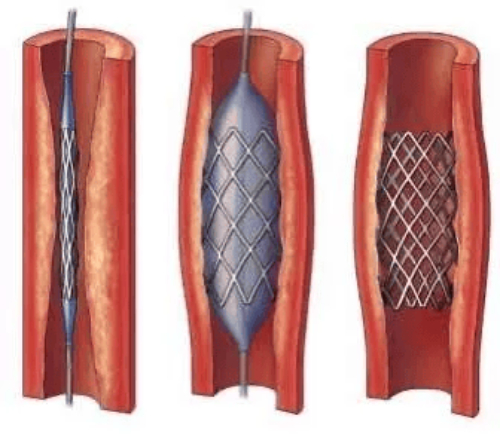
Fig. 3 Despliegue de un stent de nitinol
2 Fundamentos de las aleaciones biomédicas con memoria de forma
2.1 Principales tipos y componentes
Las aleaciones basadas en níquel-titanio, en particular el Nitinol binario (NiTi) con composición casi equiatómica (50 at.% Ni-Ti), constituyen la piedra angular de los SMA médicos debido a su superelasticidad intrínseca (∼8% de deformación de recuperación) y a su memoria de forma activada térmicamente. Los sistemas de aleaciones ternarias se diseñan para abordar las limitaciones clínicas: NiTiNb amplía la histéresis de transformación (ΔT≈30-100°C) para mejorar la estabilidad dimensional en dispositivos de fijación ósea, resistiendo las fluctuaciones térmicas; NiTiCu estrecha la histéresis (ΔT≈2-10°C) para un control preciso de la respuesta mecánica, permitiendo el ajuste de la fuerza radial a escala milimétrica en stents vasculares; NiTiCr eleva el potencial de picadura (+0,2V) y refuerza las capas de pasivación para suprimir la liberación de iones de níquel, mitigando los riesgos de alergia. En cambio, las aleaciones con base de cobre (p. ej., Cu-Al-Ni, Cu-Zn-Al) ofrecen rentabilidad y temperaturas de transición sintonizables, pero adolecen de fragilidad intergranular (vida a la fatiga <10^4 ciclos) y liberación de iones de cobre citotóxicos, lo que impide su uso en implantes. Los sistemas basados en hierro (p. ej., Fe-Mn-Si) presentan una alta resistencia y son asequibles; sin embargo, su baja deformación de recuperación (<2%) y la ausencia de superelasticidad reversible restringen sus aplicaciones a dispositivos exploratorios, no portadores de carga, sin que hasta la fecha se haya producido una traducción clínica significativa.
Tabla 1 Comparación de las propiedades de las aleaciones con memoria de forma fabricadas con distintos materiales
|
Clasificación |
Aleaciones típicas |
Características principales Dirección de optimización |
Valor médico y limitaciones |
|
Aleación a base de níquel-titanio (a base de NiTi) |
NiTi binario |
Superelasticidad (~8% de deformación de recuperación) Efecto de memoria de forma (activación por temperatura Af) |
Material de uso clínico corriente con buena biocompatibilidad (la barrera TiOx superficial evita la liberación de níquel) |
|
Aleación con base de cobre (con base de Cu) |
NiTiNb |
Ampliación de la temperatura de retardo de transición de fase (ΔT≈30-100℃) |
Mejora de la estabilidad dimensional de los implantes (como antiaflojamiento de tornillos ortopédicos) |
|
NiTiCu |
Reducir el efecto de retardo (ΔT≈2-10℃) |
Mejora de la precisión de la respuesta mecánica (fuerza radial controlada de stents vasculares) |
|
|
NiTiCr |
Mayor resistencia a la corrosión (potencial de picadura ↑0,2V) Inhibe la precipitación de iones de níquel |
Reduce el riesgo de toxicidad del implante a largo plazo (especialmente para pacientes alérgicos al níquel) |
|
|
Cu-Al-Ni |
Bajo coste Alta temperatura de cambio de fase (>100℃) |
Limitaciones: Fragilidad del límite cristalino → baja vida a la fatiga (<10^4 ciclos). Toxicidad por iones de cobre → inflamación tisular (clínicamente prohibida). |
|
|
Cu-Zn-Al |
Excelente rendimiento de procesamiento Temperatura de transición de fase ajustable (-50~100℃) |
||
|
Aleación a base de hierro |
Fe-Mn-Si |
Alta resistencia (>500MPa) Bajo coste |
Limitaciones: Deformación de recuperación baja (<2%) → fallo funcional. La transición de fase es irreversible → sin superelasticidad (limitado a dispositivos de un solo uso) |
2.2 Características principales y mecanismos
La transformación de fase martensítica es una transformación de fase no difusiva, también conocida como transformación de fase de tipo desplazamiento. En sentido estricto, en una transformación de fase de tipo desplazamiento, sólo se considera transformación de fase martensítica cuando el desplazamiento atómico se produce mediante deformación por cizallamiento y la interfaz entre las dos fases se mantiene mediante deformación elástica macroscópica para garantizar la continuidad y la congruencia, y la energía de deformación es suficiente para alterar la cinética de transformación de fase y la morfología de los productos de transformación de fase. Basándose en las definiciones de transformación de fase martensítica propuestas por numerosos estudiosos en el pasado, Xu Zuyao propuso la siguiente definición simple: una transformación de fase en la que los átomos se sustituyen sin difusión (es decir, la composición permanece inalterada, y las relaciones entre átomos vecinos permanecen inalteradas) y cizallamiento (es decir, la fase madre y la martensita están en una relación posicional), alterando así su forma. Aquí, transformación de fase se refiere a transformaciones de fase de primer orden (caracterizadas por cambios bruscos de calor y volumen, como reacciones exotérmicas y expansión) que implican nucleación y crecimiento.
La martensita se descubrió por primera vez en el acero: cuando el acero se calienta a cierta temperatura y luego se enfría rápidamente, forma una estructura templada que endurece y refuerza el acero. En 1895, el francés Osmont bautizó esta estructura con el nombre de martensita en honor del metalúrgico alemán Martens. Inicialmente, sólo se denominaba transformación martensítica a la transformación de fase de austenita a martensita en el acero. Desde el siglo XX, se han acumulado amplios conocimientos sobre las características de las transformaciones de fase martensítica en el acero. Posteriormente, se descubrió que ciertos metales puros y aleaciones también presentan transformaciones de fase martensítica, como: Ce, Co, Hf, Hg, La, Li, Ti, Tl, Pu, V, Zr, y Ag-Cd, Ag-Zn, Au-Cd, Au-Mn, Cu-Al, Cu-Sn, Cu-Zn, In-Tl, Ti-Ni, etc. Los productos de las transformaciones de fase con características básicas similares a las transformaciones de fase martensítica se denominan colectivamente martensita.
Las transformaciones de fase martensítica presentan efectos térmicos y volumétricos, y el proceso de transformación implica la formación y el crecimiento de núcleos. Sin embargo, no existe un modelo completo que explique cómo se forman y crecen estos núcleos. La velocidad de crecimiento de la martensita suele ser elevada, alcanzando en algunos casos hasta 10 cm-s. Se especula que la configuración de los defectos cristalinos (como las dislocaciones) en la fase madre influye en la nucleación de la martensita. Sin embargo, actualmente las técnicas experimentales no permiten observar la configuración de las dislocaciones en la interfaz de fase, por lo que el proceso completo de transformación de fase martensítica sigue sin estar claro. Sus características pueden resumirse como sigue:
La transformación de fase martensítica es una de las transformaciones de fase no difusivas. Durante la transformación, no se produce un desplazamiento aleatorio ni un salto ordenado de los átomos a través de la interfaz. Por lo tanto, la nueva fase (martensita) hereda la composición química, el orden atómico y los defectos cristalinos de la fase madre. Durante la transformación de fase martensítica, los átomos sufren un desplazamiento ordenado mientras mantienen sus posiciones relativas con los átomos vecinos. Este desplazamiento es de tipo cizallamiento. El resultado del desplazamiento atómico es la tensión (o deformación) de la red. Este desplazamiento por cizallamiento no sólo altera la estructura reticular de la fase madre, sino que también provoca cambios macroscópicos de forma. Si primero se traza una línea recta en la superficie de una probeta pulida, como PQRS en la Figura 3a, y parte de la probeta (A1B1C1D1-A2B2C2D2) sufre una transformación de fase martensítica (formando martensita), entonces la línea recta PQRS se pliega en tres líneas rectas conectadas: PQ, QR' y R'S'. Los planos A1B1C1D1 y A2B2C2D2 de la interfaz bifásica permanecen sin deformación y sin rotación, lo que se denomina plano habitual (de precipitación). Este cambio de forma se denomina deformación constante del plano (figura 3). El cambio de forma provoca la formación de protuberancias en la superficie de la probeta, que se ha pulido previamente. Las protuberancias superficiales de la martensita en el acero con alto contenido en carbono pueden observarse cuando se forma la martensita, produciéndose una inclinación en la superficie que se cruza con la martensita. Bajo un microscopio de interferencia, se puede ver la altura de las protuberancias y sus bordes afilados.
El efecto de memoria de forma se refiere al fenómeno en el que, tras la deformación de una aleación que experimenta una transformación de fase martensítica, cuando se calienta hasta la temperatura de terminación de la transformación de fase austenítica (Af), la martensita de baja temperatura revierte a la fase madre de alta temperatura y vuelve a su forma original antes de la deformación, o durante el enfriamiento posterior, vuelve a la forma martensítica mediante la liberación de energía elástica interna. Se trata de un material sólido con una forma determinada que, tras sufrir una deformación plástica en determinadas condiciones, vuelve completamente a su forma original antes de la deformación cuando se calienta a una temperatura determinada. Es decir, puede recordar la forma de la fase madre.
La transformación martensítica constituye el fundamento físico del efecto de memoria de forma mediante un mecanismo termoelástico de reconstrucción cristalina reversible. Al enfriarse por debajo de la temperatura de inicio de la martensita (Ms), la fase de austenita de alta temperatura (red cúbica) experimenta un cizallamiento sin difusión para formar martensita metaestable (red monoclínica/hexagonal), generando maclas autoacomodantes sin cambio macroscópico de forma. Una tensión externa inferior a Mf induce la migración de los límites de las maclas y la reorientación de las variantes, produciendo deformaciones pseudoplásticas de hasta el 8%. El calentamiento posterior por encima de la temperatura de inicio de la austenita (As) desencadena el desplazamiento cooperativo atómico para la transformación inversa, en la que la recuperación de la estructura cristalina impulsa la restauración macroscópica de la forma, la esencia del efecto de memoria de forma. Este proceso se basa en tres atributos críticos:
① Reversibilidad (una energía de distorsión de la red ΔG cercana a cero garantiza la unicidad de la trayectoria);
② Estrecha histéresis (10-30°C en aleaciones NiTi permite una activación precisa a temperatura corporal);
③ Deformación no destructiva (la macla sustituye al deslizamiento de dislocaciones para evitar daños permanentes). Desde el punto de vista médico, este mecanismo permite que los stents autoexpandibles recuperen configuraciones predefinidas a temperatura corporal, mientras que la reordenación martensítica de las maclas absorbe las vibraciones fisiológicas de la carga (por ejemplo, un 50% más de amortiguación en alambres de ortodoncia). Su estabilidad cíclica (>10^7 ciclos) garantiza además la fiabilidad a largo plazo en implantes como las válvulas cardíacas.
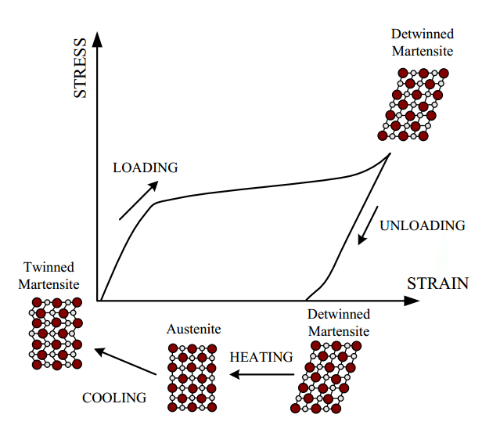
Fig. 4 Efecto de memoria de forma
2.3 Parámetros clave de rendimiento
La viabilidad clínica de las aleaciones médicas de NiTi depende de la sinergia entre biocompatibilidad, propiedades mecánicas, procesos de fabricación y compatibilidad con la esterilización. Según la norma ISO 10993, la biocompatibilidad se centra en la supresión de la liberación de iones de níquel (la pasivación superficial con TiO2 reduce la lixiviación a <0,1 μg/cm^2/semana), validada por la citotoxicidad (>90% de viabilidad celular), la sensibilización (≥95% de pruebas de parche negativas) y la hemólisis (<5%). Las propiedades mecánicas deben estar en consonancia con las exigencias de implantación: los stents cardiovasculares requieren una vida a la fatiga por flexión rotativa ultraelevada (>4×10^8 ciclos a 37 °C), mientras que los implantes articulares exigen resistencia al desgaste (<0,1 mm3/Mc de tasa de desgaste); la rigidez superelástica (0,5-3 GPa) debe coincidir exactamente con la mecánica del tejido huésped. En la fabricación se emplea la refusión por arco en vacío (VAR) para mejorar la pureza (tamaño de inclusión ≤5 μm), el estirado en frío + envejecimiento para ajustar las temperaturas de transformación (Af±2°C), y el corte por láser/electropulido para conseguir características a escala micrométrica (stent struts 80-150 μm) con baja rugosidad (Ra<0,05 μm). La esterilización final (óxido de etileno/irradiación gamma) debe limitar la desviación de la transición de fase a <1 °C sin comprometer la funcionalidad.
3 Aplicaciones en el campo biomédico
3.1 Ortopedia
En la actualidad, la cirugía ortopédica utiliza principalmente placas de acero fijas de aleación de titanio. Sin embargo, la aleación de titanio carece de propiedades autoadaptativas y superelásticas, y su ajuste a los huesos no es óptimo. En cambio, las aleaciones de níquel-titanio con memoria de forma impresas en 4D, con sus capacidades autoadaptativas, pueden lograr un ajuste relativamente perfecto con los huesos, al tiempo que ofrecen funciones tanto de soporte como de reparación.
Estos materiales de reparación ortopédica de aleaciones con memoria de forma no son meras placas planas, sino que sus superficies están densamente perforadas con pequeños orificios que facilitan el intercambio de nutrientes y favorecen el crecimiento y la reparación ósea. Múltiples componentes adaptativos de níquel-titanio impresos en 4D se han implantado clínicamente en pacientes voluntarios con tumores óseos, con resultados clínicos prometedores.
En la reparación de defectos óseos se utilizan andamios de NiTi de estructura porosa graduada, con una resistencia a la tracción de 625,6 MPa, un índice de elongación del 14,67% y un índice de recuperación de la deformación del 99,51%. El refuerzo de grano fino (tamaño de grano ~20,5 μm) sinergiza con la densidad de dislocación para lograr la absorción de energía bajo grandes esfuerzos. Sustitución y reparación de articulaciones: dispositivos de fijación de cazoletas acetabulares, componentes de articulaciones artificiales (en fase de exploración, centrados en el desgaste y la fatiga) y rellenos de defectos óseos (SMA poroso).
En el campo de la cirugía de la columna vertebral, las aleaciones con memoria de forma (SMA), especialmente las aleaciones de níquel-titanio (NiTi), han impulsado innovaciones en ortopedia dinámica y técnicas de fusión mínimamente invasivas. Las barras ortopédicas de NiTi consiguen una corrección precisa gracias a un efecto de memoria de forma de doble fase: a bajas temperaturas, en la fase martensítica, las barras sufren una deformación plástica para adaptarse a los procedimientos quirúrgicos; una vez implantadas en el cuerpo, la temperatura corporal desencadena una transformación en fase austenítica, restaurando la curvatura preestablecida y aplicando continuamente una fuerza correctora axial (por ejemplo, una barra de 6 mm de diámetro genera aproximadamente 200 N de fuerza a 40 °C, mientras que una de 9 mm alcanza los 500 N). Los experimentos con animales (modelos caprinos) demostraron que las barras de NiTi precurvadas podían reducir los ángulos de escoliosis de 41° a 11° sin causar lesiones nerviosas; los estudios con cadáveres humanos confirmaron además su capacidad para corregir simultáneamente las deformidades coronales, sagitales y rotacionales. En cuanto al diseño de la innovación clínica, las varillas rectangulares/cuadradas mejoran la capacidad antirrotacional, corrigiendo el ángulo de Cobb de 57,8° a 17,8° sin que se observen recidivas durante un periodo de seguimiento de 4 años; el sistema activado por temperatura corporal utiliza pulsos de radiofrecuencia (450 Hz) para inducir el calentamiento local, evitando los riesgos asociados al daño térmico tradicional.
El desarrollo de dispositivos de fusión intervertebral se centra en la implantación mínimamente invasiva y la estabilidad a largo plazo. Aprovechando las propiedades de transformación de fase del NiTi, el dispositivo de fusión puede sufrir una deformación por compresión en un estado martensítico a baja temperatura (por ejemplo, en un entorno de agua helada) y recuperar automáticamente su altura original tras la implantación en el espacio intervertebral mediante la transformación de fase austenítica desencadenada por la temperatura corporal. En cuanto a la optimización de la estructura porosa, las redes en forma de diamante (porosidad del 70-72%, red unitaria de 1,5 mm) producidas mediante tecnología de fusión selectiva por láser (SLM ) favorecen significativamente el crecimiento vascular. La zona de contacto está diseñada con una fase martensítica (bajo módulo elástico) para reducir eficazmente el apantallamiento de la tensión de la placa terminal. Además, la estructura de "dientes de bloqueo" en los bordes del dispositivo de fusión se incrusta en las placas terminales durante la recuperación de la forma, logrando una resistencia antidesplazamiento de 1800 N, eliminando la necesidad de tornillos o varillas auxiliares para la fijación y simplificando aún más el procedimiento quirúrgico.
En el campo del tratamiento de fracturas, las aleaciones con memoria de forma (SMA) han mejorado significativamente los resultados de la fijación y el pronóstico de los pacientes gracias a la compresión dinámica, la implantación mínimamente invasiva y la tecnología de adaptación biomecánica. Los clavos intramedulares de compresión continua utilizan el efecto de memoria de forma de doble etapa de la aleación NiTi. Tras ser predeformados en estado martensítico a baja temperatura, se implantan en la cavidad medular. Al recalentarse a la temperatura corporal, recuperan su forma original y generan una tensión de compresión axial (0,5-1 MPa), acelerando así la formación del callo óseo. Estudios clínicos comparativos demuestran que, en comparación con las placas de acero tradicionales, el grupo de clavos intramedulares NiTi reduce el tiempo de consolidación de la fractura en un 25% y la tasa de no unión al 0,9%. Sus características mínimamente invasivas (por ejemplo, implantación a través de una incisión de 2 cm para fracturas de extremidades pediátricas, con un diámetro seleccionado a 2/5 del punto más estrecho de la cavidad medular) mejoran aún más la amplitud de movimiento articular postoperatoria en un 30%.
Los tornillos óseos autocompactantes y los injertos óseos consiguen una fijación activa mediante un mecanismo de cambio de fase. El tornillo óseo se atornilla en el hueso en estado martensítico y, tras el recalentamiento, se expande radialmente, aumentando la tensión de la interfaz en un 40% y mejorando significativamente la fuerza de sujeción; cuando se utiliza el fijador de anillo de TiNi para la fijación esternal, la puntuación del dolor postoperatorio VAS disminuye a 5,17 ± 1,14 (7,65 ± 1,08 en el grupo tradicional). La estancia hospitalaria se acorta en 6 días. Además, los fijadores óseos biodegradables de aleación de magnesio (con un módulo elástico de 45 GPa, similar al del hueso cortical) se alinean con el ciclo de curación ósea (tasa de curación del 100% a los 6 meses de seguimiento), eliminando la necesidad de una cirugía de extracción secundaria y proporcionando una nueva dirección para la aplicación práctica de materiales biodegradables en la fijación de fracturas.
Las placas de compresión de bloqueo (LCP) optimizadas con NiTi abordaron los retos de fijación en pacientes osteoporóticos mediante un diseño biomecánicamente adaptado. En combinación con la tecnología de implantes mínimamente invasiva (MIPPO), las placas LCP precurvadas se insertan por vía submuscular y se fijan con tornillos percutáneos, lo que reduce la interrupción del riego sanguíneo en un 70% y resulta especialmente adecuado para fracturas en zonas con escaso riego sanguíneo, como la parte distal de la tibia.
Las aleaciones con memoria de forma (SMA) han logrado avances revolucionarios en ortopedia, desde la corrección dinámica hasta la biocompatibilidad, gracias a su efecto único de memoria de forma y su superelasticidad. En la corrección de la columna vertebral, las aleaciones de NiTi consiguen un tratamiento preciso mediante un efecto de memoria de forma de doble fase: las barras de corrección con deformación plástica en estado martensítico a baja temperatura se implantan a través de túneles subcutáneos, y la temperatura corporal desencadena una transformación de fase austenítica para restaurar la curvatura preestablecida, generando 200-500 N de fuerza correctora axial (diámetro 6-9 mm). Combinado con un diseño rectangular/cuadrado para mejorar la capacidad antirrotación (por ejemplo, el sistema Wang reduce el ángulo de Cobb de 57,8° a 17,8°), corrige simultáneamente las deformidades coronales, sagitales y rotacionales; la tecnología de calentamiento por impulsos de radiofrecuencia (450 Hz) minimiza aún más el riesgo de lesiones térmicas. Los dispositivos de fusión intervertebral utilizan propiedades de transformación de fase para una implantación mínimamente invasiva: tras la compresión a baja temperatura, el volumen se reduce en un 40%, y tras la implantación en el espacio intervertebral, la altura se restablece automáticamente; la estructura porosa en forma de diamante (porosidad del 70-72%) preparada mediante fusión selectiva por láser favorece el crecimiento vascular, la zona de contacto martensítica reduce el blindaje de la tensión de la placa terminal, y los "dientes de bloqueo" del borde proporcionan 1800 N de resistencia antidesplazamiento sin necesidad de fijación auxiliar.
En el campo de la fijación de fracturas, los SMA optimizan significativamente la eficacia terapéutica mediante la compresión dinámica y la adaptación biomecánica. Los clavos intramedulares de NiTi predeformados vuelven a su estado original a temperatura corporal, generando una tensión de compresión axial de 0,5-1 MPa, lo que acelera la formación de callo (el tiempo de curación se reduce en un 25%, la tasa de no unión es del 0,9%); los clavos intramedulares elásticos implantados a través de una incisión de 2 cm en fracturas de extremidades pediátricas mejoran la amplitud de movimiento articular en un 30% en el postoperatorio. Los tornillos óseos de autocompresión utilizan la transformación de fase martensita-austenita para lograr la expansión radial (la tensión de la interfaz aumenta en un 40%); los fijadores anulares de TiNi reducen las puntuaciones de la EAV a 5,17 ± 1,14 tras la cirugía de fijación esternal (grupo tradicional: 7,65 ± 1,08), con una reducción de 6 días en la estancia hospitalaria; los fijadores óseos biodegradables de aleación de magnesio (módulo elástico 45 GPa) se absorben completamente en 6 meses, logrando una tasa de curación del 100% y evitando la necesidad de cirugía secundaria. Las placas de compresión de bloqueo optimizadas para NiTi reducen la densidad de los tornillos en un 50% gracias al bloqueo cortical único (para pacientes osteoporóticos) y, combinadas con la tecnología MIPPO, reducen la interrupción del riego sanguíneo en un 70%, lo que las hace adecuadas para fracturas complejas como las de tibia distal.
Las principales ventajas residen en la profunda integración de las propiedades de los materiales y las necesidades clínicas: la implantación mínimamente invasiva (barras de corrección espinal a través de túneles subcutáneos, dispositivos de fusión con un volumen reducido en un 40%) reduce el riesgo de lesión nerviosa; la tensión compresiva dinámica (expresión de BMP-2 multiplicada por 2) y la amortiguación superelástica (amplitud de vibración 50% del acero inoxidable) optimizan el microentorno de curación ósea; los dispositivos de fusión de NiTi poroso (módulo elástico 25-90 GPa) y las aleaciones de magnesio biodegradables (100% de transferencia de carga al hueso nuevo) reducen significativamente el apantallamiento de la tensión. Estas innovaciones logran un salto de la fijación pasiva a la regulación activa y del soporte rígido a la biocompatibilidad mediante mecanismos de cambio de fase, optimización estructural y tecnología biodegradable, proporcionando soluciones más seguras y eficaces para el tratamiento de enfermedades esqueléticas complejas.
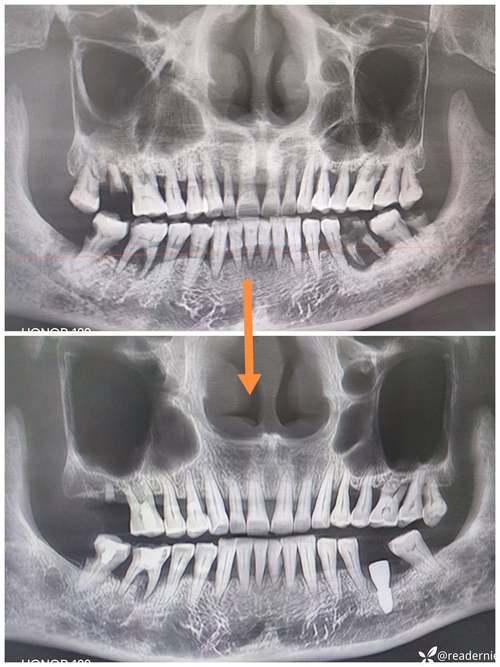
Fig. 5 Radiografía de escoliosis con barra espinal de nitinol
3.2 Intervenciones cardiovasculares
En el campo de las intervenciones cardiovasculares, las aleaciones con memoria de forma (SMA) han impulsado innovaciones tecnológicas en stents vasculares, oclusores y filtros aprovechando su superelasticidad y sus efectos de memoria de forma. Los stents vasculares autoexpandibles, una aplicación típica de la superelasticidad, aprovechan las propiedades de transformación de fase de las aleaciones de NiTi para permitir un tratamiento mínimamente invasivo: el stent se comprime en el sistema de colocación (diámetro 1-2 mm) en su estado martensítico a baja temperatura, y luego se coloca mediante un catéter en el lugar afectado. La temperatura corporal desencadena la transformación en fase austenítica, lo que hace que el stent recupere automáticamente su diámetro preestablecido (por ejemplo, una fuerza de apoyo radial de 0,35 N/mm para los stents coronarios), eliminando la necesidad de expandir el balón a alta presión. Su flexibilidad se optimiza mediante procesos de corte o tejido por láser, con una rigidez a la flexión tan baja como 0,3-0,5 N-m^2, lo que permite su adaptación a estructuras anatómicas complejas como el arco aórtico. Además, la resistencia a la fatiga de las aleaciones de NiTi (por ejemplo, la endoprótesis Eduratec soporta 100 millones de ciclos pulsátiles) garantiza la estabilidad a largo plazo, lo que la hace adecuada para diversas localizaciones, como los vasos periféricos, las arterias coronarias, los vasos cerebrales y la aorta.
El oclusor utiliza el efecto de memoria de forma de doble fase de la AMS para lograr un tratamiento preciso: Los oclusores de comunicación interauricular, foramen oval permeable o conducto arterioso permeable presentan una forma lineal recta en estado martensítico a baja temperatura. Una vez introducidos en la cavidad cardiaca a través de un catéter, la temperatura corporal desencadena su restauración en una estructura de disco-cintura-disco, con la cintura incrustada en el lugar del defecto y los discos dobles anclando las aurículas/arterias izquierda y derecha, logrando una oclusión mínimamente invasiva. Los datos clínicos demuestran que los oclusores de NiTi pueden reducir las puntuaciones de dolor postoperatorio VAS en pacientes con conducto arterioso persistente a 2,1 ± 0,8 (frente a 5,3 ± 1,2 con la cirugía tradicional) y acortar la estancia hospitalaria a 3 días. Su diseño superelástico (con una tasa de recuperación de la deformación del 99,2%) puede adaptarse a la deformación dinámica de la contracción y relajación cardiacas, reduciendo el riesgo de derivación residual.
El filtro de vena cava inferior optimiza el tratamiento de la tromboembolia venosa gracias a la resistencia de la aleación de NiTi a la flexión y a la capacidad de captura del trombo: el filtro permanece comprimido dentro de la vaina de liberación y, al soltarse, confía en su superelasticidad para restaurar su estructura en forma de paraguas. El diseño de la abertura de la malla del filtro (normalmente de 1-2 mm) puede interceptar más del 95% de los trombos, permitiendo al mismo tiempo un flujo sanguíneo normal. La resistencia a la fatiga de la aleación de NiTi (por ejemplo, tasa de fractura del filtro <1% a los 5 años de seguimiento) garantiza la seguridad a largo plazo, mientras que su bajo módulo elástico (40-60 GPa) reduce la irritación de la pared vascular y disminuye la incidencia de flebitis.
Estos dispositivos logran una transición del soporte pasivo a la adaptación activa y de la cirugía abierta a la intervención mínimamente invasiva mediante el mecanismo de cambio de fase y la optimización estructural del SMA. Sus principales ventajas son: un equilibrio entre flexibilidad y fuerza de soporte radial gracias a la superelasticidad (por ejemplo, rigidez de flexión de la endoprótesis coronaria de 0,4 N-m^2, fuerza radial de 0,35 N/mm), posicionamiento y despliegue precisos gracias a los efectos de la memoria de forma (por ejemplo, error de posicionamiento del oclusor <1 mm) y estabilidad a largo plazo gracias a la adaptación biomecánica (por ejemplo, tasa de permeabilidad del filtro del 98% tras 5 años). Estas innovaciones ofrecen opciones de tratamiento más seguras y eficaces para las enfermedades cardiovasculares.
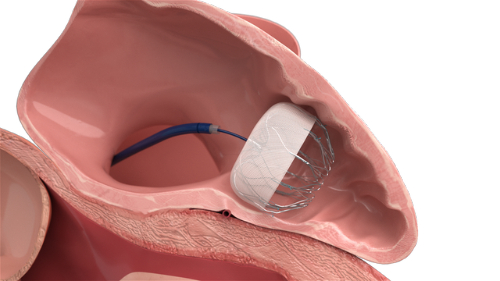
Fig. 6 Oclusor cardíaco
3.3 Odontología
En el campo de la medicina oral, las aleaciones con memoria de forma (SMA) han impulsado innovaciones tecnológicas en ortodoncia, endodoncia, prostodoncia y cirugía maxilofacial debido a su superelasticidad y biocompatibilidad. Los arcos de ortodoncia, una de las aplicaciones más consolidadas, utilizan la superelasticidad de las aleaciones de NiTi para proporcionar fuerzas correctoras continuas y suaves (0,5-1,5 N), reduciendo significativamente la frecuencia de las visitas de seguimiento (los datos clínicos muestran que los intervalos de seguimiento pueden ampliarse a 8-12 semanas, una mejora del 40% con respecto a los alambres tradicionales de acero inoxidable), al tiempo que mejoran la comodidad del paciente (las puntuaciones de la Escala Visual Analógica [EVA] se reducen a 2,3 ± 0,6, frente a 4,8 ± 1,1 de los alambres tradicionales). Los alambres con diferentes temperaturas de transición de fase pueden adaptarse a las diferentes etapas del tratamiento: los alambres de fase martensítica de baja temperatura (Af < 25°C) son adecuados para la etapa inicial de alineación, utilizando una baja rigidez (módulo elástico de 28 GPa) para reducir el daño del ligamento periodontal; los alambres de fase austenítica (Af > 35°C) proporcionan una fuerza ortodóncica estable en etapas posteriores, garantizando la eficacia del tratamiento mediante una tasa de recuperación de la deformación del 99,3%.
Las limas radiculares de NiTi optimizan la seguridad del tratamiento gracias a su superelasticidad: Las limas tradicionales de acero inoxidable, debido a su elevada rigidez, son propensas a la desviación del conducto radicular (tasa de incidencia del 12-18%) y a la rotura de la aguja (riesgo del 3-5%). En cambio, las propiedades de transformación de fase martensítica de las limas NiTi triplican la flexibilidad en los conductos radiculares curvos, lo que permite su adaptación a conductos con curvaturas superiores a 30°, reduciendo significativamente las tasas de desviación (<2%) y de rotura de agujas (<0,5%). Los estudios clínicos demuestran que la tasa de éxito del tratamiento de conductos radiculares en una sola visita utilizando limas NiTi alcanza el 92%, lo que supone una mejora del 25% con respecto a las limas de acero inoxidable, especialmente indicadas para conductos radiculares calcificados o estrechos.
Los ganchos y conectores de NiTi en la restauración de prótesis logran un equilibrio entre la fuerza de retención y la comodidad gracias a su superelasticidad: El gancho es fácil de ajustar en el estado martensítico a baja temperatura y vuelve a su forma preestablecida después del recalentamiento mediante la transformación de fase austenítica, aumentando la fuerza de retención a 3-5 N (en comparación con 1-2 N para las aleaciones tradicionales de cobalto-cromo). Además, el bajo módulo elástico (40-60 GPa) reduce la presión sobre las encías (distribución más uniforme de la presión, con una reducción del 60% del índice de irritación de la mucosa). El conector presenta un diseño de estructura tejida con una excelente resistencia a la fatiga (sin fracturas tras 10^5 ciclos), lo que lo hace adecuado para sistemas de fijación de precisión en prótesis parciales removibles.
En cirugía maxilofacial, las férulas de fijación de fracturas y los dispositivos de tracción utilizan el efecto de memoria de forma del SMA para un tratamiento mínimamente invasivo: la férula se moldea a bajas temperaturas para ajustarse a la superficie ósea y, al recalentarse, la transformación de fase genera una fuerza de fijación de 50-100 N, evitando los daños en los tejidos blandos causados por la ligadura tradicional con alambre; el dispositivo de tracción consigue un ajuste progresivo del segmento óseo mediante el control periódico de la temperatura (por ejemplo, activación a 40°C y relajación a 20°C). Los casos clínicos demuestran que el tiempo de curación de la fractura mandibular se reduce a 6 semanas (8-10 semanas con los métodos tradicionales), y no se requiere cirugía secundaria para retirar los dispositivos de fijación interna.
Las aplicaciones mencionadas logran un salto de la adaptación pasiva a la regulación activa y de los dispositivos rígidos a la adaptación flexible gracias a la profunda integración del mecanismo de transición de fase de SMA con las necesidades clínicas. Sus principales ventajas son: fuerza suave y sostenida proporcionada por la superelasticidad (error de fuerza de corrección ortodóncica <0,2N), recuperación precisa de la forma lograda mediante efectos de memoria de forma (error de posicionamiento del anillo <0,5 mm) y mayor seguridad del tratamiento mediante la adaptación biomecánica (tasa de rotura de la aguja de tratamiento del conducto radicular <0,5%). Estas innovaciones ofrecen soluciones más eficaces y cómodas para el tratamiento de las enfermedades bucodentales.

Fig. 7 Lima endodóntica de nitinol
3.4 Radiología intervencionista y cirugía mínimamente invasiva
En los procedimientos intervencionistas mínimamente invasivos y en las operaciones quirúrgicas, las aleaciones con memoria de forma (SMA) mejoran significativamente la maniobrabilidad y adaptabilidad de los dispositivos médicos gracias a sus efectos de superelasticidad y memoria de forma. Las guías y catéteres superelásticos, que aprovechan las propiedades de transformación de fase de las aleaciones de NiTi, demuestran un rendimiento excepcional en estructuras anatómicas complejas: Las guías presentan una gran flexibilidad (radio de curvatura <1 mm) en estado martensítico a baja temperatura, lo que permite su adaptación al recorrido en espiral de 360° de las arterias coronarias; tras el recalentamiento, la transformación en fase austenítica confiere una gran tenacidad a la fractura (deformación de fractura >8%), combinada con el diseño en forma de "J" del extremo distal de la guía, lo que permite un control preciso del par de torsión (eficiencia de transmisión del par de torsión de hasta el 95%). El catéter optimiza la flexibilidad de la punta gracias a la tecnología de corte por láser, lo que permite que un catéter de 5F atraviese sin problemas el segmento tortuoso de la arteria carótida (radio de curvatura de 2 mm). El andamio superelástico proporciona suficiente soporte (resistencia axial 12 N) para evitar el daño vascular causado por el "efecto boca de pez".
Los instrumentos de agarre y extracción de cálculos, como las cestas para cálculos y las pinzas para cuerpos extraños, utilizan el efecto de memoria de forma de doble etapa del SMA para procedimientos mínimamente invasivos: Los instrumentos mantienen una forma lineal recta en estado martensítico a baja temperatura. Una vez introducidos en el lugar de destino a través del canal endoscópico, la temperatura corporal provoca su restauración a la estructura de cesta preestablecida (por ejemplo, diseño de cuatro garras), lo que permite la recuperación de cálculos o cuerpos extraños con diámetros de entre 2 y 10 mm. La tasa de recuperación de la deformación alcanza el 99,5%, lo que garantiza una tasa de éxito de la recuperación única superior al 90%. Los datos clínicos demuestran que la litotricia ureteroscópica (URSL) con cestas para cálculos de NiTi reduce el tiempo de intervención a 25 minutos (frente a 40 minutos con los métodos tradicionales), con una tasa de cálculos residuales postoperatorios <5%.
Las bobinas de embolización de aneurismas optimizan la eficacia del empaquetamiento mediante efectos parciales de memoria de forma: Las bobinas se comprimen dentro del microcatéter (diámetro de 0,015-0,021 pulgadas) y, al soltarse, se adaptan a la morfología de la cavidad del aneurisma mediante superelasticidad (densidad de empaquetamiento >30%). Además, la fuerza de restauración generada por la transformación de fase martensítica reduce el riesgo de desplazamiento de la bobina (tasa de recurrencia <2% a 1 año de seguimiento). En los aneurismas de cuello ancho, las bobinas de NiTi con una estructura tridimensional tejida pueden formar una "cesta" estable, combinada con la tecnología asistida por stent, para aumentar la densidad de embolización hasta el 95%.
Los endoscopios deformables y los retractores autoexpandibles simplifican el proceso quirúrgico gracias a la capacidad de deformación activa de la SMA: la sección de inserción del endoscopio utiliza una estructura de tubo en espiral de aleación de NiTi que vuelve automáticamente a un ángulo de flexión preestablecido (por ejemplo, 90°) a la temperatura corporal, reduciendo la necesidad de ajustes manuales de flexión por parte del cirujano; el retractor autoexpandible se comprime y se carga a bajas temperaturas y, al soltarse, expande rápidamente el campo quirúrgico utilizando superelasticidad (tiempo de expansión <5 segundos), evitando la compresión tisular continua causada por los retractores tradicionales (con una mejora del 40% en la uniformidad de la distribución de la presión). Estos diseños aumentan el espacio operatorio en un 30% en la colecistectomía laparoscópica (CL) y otras cirugías, reduciendo el tiempo quirúrgico a 35 minutos (50 minutos con los métodos tradicionales).
Los citados instrumentos logran un salto del funcionamiento pasivo a la adaptación activa y del control lineal a la regulación tridimensional mediante la profunda integración del mecanismo de cambio de fase de SMA con las necesidades clínicas. Sus principales ventajas son: una combinación equilibrada de propiedades antipliegue y flexibilidad proporcionada por la superelasticidad (tensión de rotura del alambre del 8% frente al 3% del acero inoxidable), una recuperación precisa de la forma lograda mediante efectos de memoria de forma (error de posicionamiento de la cesta de cálculos <1 mm) y efectos mínimamente invasivos posibilitados por la adaptación biomecánica (diámetro de inserción del endoscopio reducido a 2,8 mm). Estas innovaciones proporcionan soluciones más seguras y eficaces para procedimientos intervencionistas y quirúrgicos complejos.
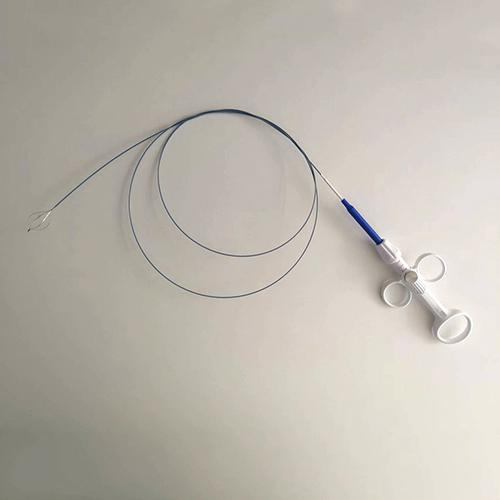
Fig. 8 Canastilla de Nitinol
6 Conclusión
Las aleaciones con memoria de forma (SMA), en particular las aleaciones de níquel-titanio (NiTi), demuestran un valor único e insustituible en el campo médico debido a su superelasticidad y efecto de memoria de forma (SME). Su superelasticidad proporciona fuerzas correctivas suaves y sostenidas -por ejemplo, los alambres de ortodoncia reducen la frecuencia de las visitas de seguimiento- y se adapta bien a estructuras anatómicas complejas, como la optimización de la flexibilidad de los stents cardiovasculares. Mientras tanto, el efecto de memoria de forma permite la implantación mínimamente invasiva y la deformación activa de dispositivos médicos. Por ejemplo, las férulas de fijación de fracturas pueden restablecer la tensión de compresión a temperatura corporal. Estas propiedades resuelven directamente los problemas clínicos, como la rigidez insuficiente, la complejidad de los procedimientos quirúrgicos y la escasa eficacia a largo plazo de los dispositivos tradicionales.
De cara al futuro, con los avances tecnológicos en AME biodegradable (como las aleaciones de magnesio) y dispositivos activos (como los dispositivos de recuperación accionados eléctricamente), la AME está preparada para desempeñar un papel más revolucionario en los dispositivos médicos inteligentes, la terapia personalizada y la cirugía mínimamente invasiva; por ejemplo, andamios impresos en 3D personalizados según la estructura anatómica del paciente e implantes inteligentes que puedan responder en tiempo real a las señales fisiológicas. Estos avances impulsarán aún más la transición de la medicina de la "reparación pasiva" a la "regulación activa", logrando en última instancia un tratamiento de las enfermedades más seguro, eficiente y personalizado.
Lectura relacionada:
El futuro es ahora: aleaciones con memoria de forma
Aleaciones con memoria de forma de Ni-Ti y sus componentes
Superelasticidad y memoria de forma del nitinol
Cómo finalizar sus demandas de Nitinol
Experimento de SAM sobre el alambre de nitinol con memoria de forma mágica
Las 6 aplicaciones médicas principales del nitinol
Referencias
[1] Kinji. Sato, Hideaki. Goto, Nobuhisa. Tomita, THE SHAPE MEMORY HEAT TREATMENT AND ENVIRONMENTAL TEMPERATURE FOR IMPROVEMENT OF FORMING LIMIT ON TI-NI BASED SHAPE MEMORY ALLOY, Editor(es): W.B. LEE, Advances in Engineering Plasticity and its Applications, Elsevier, 1993, Páginas 1117-1125, ISBN 9780444899910, https://doi.org/10.1016/B978-0-444-89991-0.50153-0.
[2] N.B Morgan, Medical shape memory alloy applications-the market and its products, Materials Science and Engineering: A, Volumen 378, Números 1-2, 2004, Páginas 16-23, ISSN 0921-5093, https://doi.org/10.1016/j.msea.2003.10.326.
[3] Tarniţă D, Tarniţă DN, Bîzdoacă N, Mîndrilă I, Vasilescu M. Properties and medical applications of shape memory alloys. Rom J Morphol Embryol. 2009;50(1):15-21. PMID: 19221641.
[4] Ward B, Parry J. Routine intramedullary screw versus plate fixation of lateral malleolus fractures. Eur J Orthop Surg Traumatol. 2025 May 31;35(1):222. doi: 10.1007/s00590-025-04341-1. PMID: 40448862.
[5] Behrang Tavousi Tehrani, Shervin Shameli-Derakhshan, Hossein Jarrahi, An overview on Active Confinement of Concrete column and piers Using SMAs. Febrero de 2017, https://www.researchgate.net/publication/310505502_An_overview_on_Active_Confinement_of_Concrete_column_and_piers_Using_SMAs

 Bares
Bares
 Cuentas y esferas
Cuentas y esferas
 Tornillos y tuercas
Tornillos y tuercas
 Crisoles
Crisoles
 Discos
Discos
 Fibras y tejidos
Fibras y tejidos
 Películas
Películas
 Escama
Escama
 Espumas
Espumas
 Folio
Folio
 Gránulos
Gránulos
 Panales
Panales
 Tinta
Tinta
 Laminado
Laminado
 Bultos
Bultos
 Mallas
Mallas
 Película metalizada
Película metalizada
 Placa
Placa
 Polvos
Polvos
 Varilla
Varilla
 Hojas
Hojas
 Cristales individuales
Cristales individuales
 Blanco para sputtering
Blanco para sputtering
 Tubos
Tubos
 Lavadora
Lavadora
 Cables
Cables
 Conversores y calculadoras
Conversores y calculadoras
 Escriba para nosotros
Escriba para nosotros
 Chin Trento
Chin Trento



